喹诺酮类药物(quinolones,QNs)是一类十分重要的人工合成的抗菌药物,对革兰氏阴性菌、大多数革兰氏阳性菌、衣原体等具有杀灭作用,广泛应用于兽医临床。
QNs属于吡酮酸衍生物(pyridonecarboxylic acids,PCAs),俗称“喹诺酮类”。1962年,美国Sterling-Winthrop研究所的Lesher等发现第一个QNs萘啶酸(nalidixic acid),通过对其进行一些结构的改变(修饰),增强了它们的生物学和药理学活性。国际学术界将QNs的发展分为四个阶段,1997年由Aandriole提出、经Schellhore整理的Aandriole-Schellhore的分类方法将QNs分为四代,如表5-16所示。
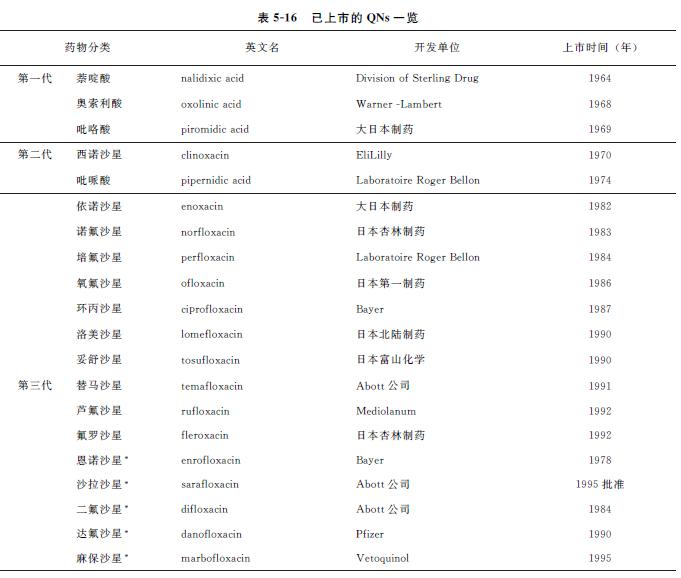

第一代QNs以萘啶酸为代表,20世纪60年代进入临床,具有中等抗菌活性,主要对革兰氏阴性菌有活性,在体内易被代谢和失活,但由于其不良反应严重,目前基本退出市场。
第二代QNs以吡哌酸为代表,20世纪70年代进入临床,与第一代QNs相比,抗菌谱更广,对铜绿假单胞菌有抗菌活性,对萘啶酸和吡咯酸有高度耐药的菌株也有活性,有很好的组织渗透性,比萘啶酸有更好的临床疗效。
第三代QNs以诺氟沙星(NOR)、环丙沙星(CIP)为代表,20世纪80年代QNs进入快速发展时期,通过化学修饰在其主环C6位引入氟原子,故被又称为“氟喹诺酮类药物(fluoroquionlones,FQs)”。FQs的问世使学术界对QNs有了全新的认识和评价,并得到了广泛的临床应用,获得了一致好评,其综合临床疗效对革兰氏阴性菌来讲,已经超过青霉素族,达到了第一代、第二代头孢菌素的效果。其由于具有口服吸收迅速、体内分布广、消除时间长、毒副作用小和无致畸性等特点,故在临床上广泛用于呼吸道、泌尿道、胆管、皮肤软组织等治疗。
*四代第**QNs是在20世纪90年代后期上市的,除具有第三代QNs的优点外,抗菌谱进一步扩展到衣原体、支原体等病原体,且对革兰氏阳性菌和厌氧菌的活性强于CIP等。此类药物具有吸收迅速、分布广泛、血药浓度大、半衰期长以及生物利用度高等优点,同时大大减少了中枢神经毒性作用,表现出与细胞色素450系统更小的相互作用。
本部分综述了QNs的理化性质、药理与毒理、危害、国内限量要求以及残留检测的样品前处理、仪器测定方法等内容,以期为该类药物的全面了解和残留检测提供参考。
1 结构与性质
QNs是以1,4-二氢4-氧吡啶-3-羧酸为基本母环结构的化合物,是由萘啶酸或吡酮酸演化而来的合成抗菌药物,其结构如表5-17所示:A环是抗菌药物必需的基本结构,变化小,而B环可做较大改变,可以是苯环、吡啶环、嘧啶环等。对FQs分子结构的某些部位,如2位的氢、3位的羧酸和4位的环外氧是很少进行修饰的。因为3位的羧酸和4位的环外氧是FQs分子结合到细菌DNA促旋酶的部分,因此不能改变这部分周围的立体化学结构;2位因非常靠近结合位点,在此的任何修饰都是很有限的。对其进行一些结构的改变(修饰)增强了它们的生物学和药理学活性。这些结构的改变包括在1号位引入烷基(烃基)或芳基,在6号位和7号位分别进行氟取代和哌嗪基取代。通过将氟取代基引入6号位,产生了FQs,从而扩大了其对革兰氏阴性和阳性菌的抗菌(活性)谱。而7号位哌嗪基的引入改善了其针对铜绿假单胞菌的抗菌活性。
N1位取代基在寻找高效、广谱QNs方面有着重要的作用。在1位上加入侧链可明显影响抗菌活性1位氮原子的取代基可以是烃基或环烃基,以乙基或乙基体积相近的取代基最好。在已用于临床的QNs中,CIP是抗肠杆菌和铜绿假单胞菌最有效的药物。左旋氧氟沙星和芦氟沙星在1和8位形成桥环,均增强了抗革兰氏阳性菌的活性。

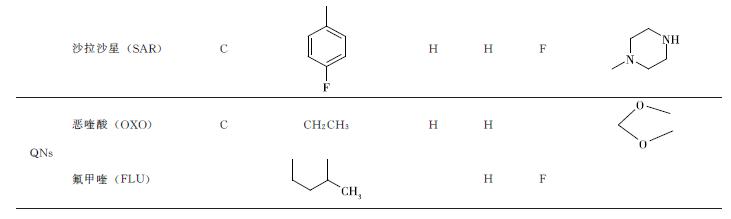
6位引入氟后增强了这些化合物抗革兰氏阴性菌的效力,并扩大了抗革兰氏阳性菌谱,与无取代的相应化合物比较,与DNA促旋酶结合能力提高了2~17倍,对细胞渗透力提高了1~70倍,因此6位上的氟称为FQs结构的显著特点。
7位的结构主要影响药物的抗菌谱、作用强度及药动学。大量的构效关系研究表明,将碱性并具有适当水溶性的取代基引入7位,均有利于提高抗菌活性和改善药动学性质。最常见的取代基是哌嗪或甲基哌嗪。哌嗪环的引入(如NOR)增强了抗铜绿假单胞菌的活性,甲基哌嗪环的引入(如PEF)则增加了药物的脂溶性,使肠道吸收能力增强,对细菌的穿透力提高。由此可见,母体环7位上以C-N键连接哌嗪基或吡咯基,与以C-C键连接吡嗪基有截然不同的抗菌活性。
QNs8位的结构改造主要影响药物的药动学性质和光毒性。多项研究结果表明,QNs的光毒性可能是由于药物对光不稳定,紫外灯照射使得药物的结构发生变化,引起药物分解所致,或由于该产物引发了氧游离基而导致光毒性。8位引入卤素可改造药物的吸收,但8位卤素引入也有可能增加药物的光毒性,8-氯喹诺酮对紫外线不稳定,有光毒性。
近年来,某些FQs因具有抗肿瘤活性已引起人们的广泛关注,氟喹诺酮类抗肿瘤药物的构效关系研究也取得了长足的进展。QNs是近年来各国竞相开发和应用的品种,已有10余种药物上市,目前国内外已批准动物专用的QNs主要有ENR、DIF、SAR、DAN、MAR等。
2 药理学
QNs主要为细菌DNA合成的*制剂抑**,作用的靶酶是DNA促旋酶。由于DNA促旋酶存在于所有的细菌中,DNA促旋酶与其他蛋白质一起催化双链DNA的超螺旋程度的改变,从而改变DNA结构。DNA促旋酶是由gyrA、gyrB两个亚单位构成的四聚体(A2B2),主要催化染色体或质粒DNA发生拓扑学转变。亚单位gyrA与DNA相联结并介导DNA链的断开和再聚合修复,而亚单位gyrB含有ATP结合部位。gyrA与DNA双链的断裂有关(由酶-DNA共价中间体介导)。在有机体内,这个过程导致两个副超螺旋和ATP的水解。QNs可以抑制DNA促旋酶gyrA亚单位,从而*制抵**细菌DNA的复制转录,使DNA、RNA、蛋白质的合成受到干扰,使细菌不能再进行分裂而起到杀菌的作用。这种作用一般对细菌的选择性高,对人的安全性大,因而QNs的发现和发展开创了合成抗菌药物的新时代。
QNs的作用特点可归结为对革兰氏阴性菌、支原体和一些革兰氏阳性菌具有强大的杀灭作用,组织渗透能力强,毒副作用低。可用于大肠杆菌、肺炎链球菌、肺炎杆菌、肺炎衣原体、金黄色葡萄球菌、肠球菌、流感杆菌、绿脓杆菌等引起的多种组织感染,如呼吸道、肠道、泌尿、皮肤和深部组织感染或败血症的治疗。
QNs为浓度依赖性抗菌药物,抗菌后效应较长(可达4~8h)。QNs口服吸收效果好,生物利用度较高,一般可达80%以上。但不同种类的动物会有明显的个体差异,通常单胃动物在口服后可以迅速吸收QNs。对反刍动物和马属动物,口服QNs后全身血药浓度要低于治疗水平的浓度。例如对于ENR,成年反刍动物的口服生物利用度只有10%,而单胃动物的口服生物利用度可达80%以上。抗菌药物在机体内的活性以及药物从血液分布到组织的能力都取决于药物的游离浓度。然而,大多数的药动学研究通常以总的药物浓度来作为所接触药物的衡量指标,如血药浓度-时间曲线下面积AUC、血药达峰浓度cmax等,很少考虑到游离药物浓度。为此,Toutain等发表了一篇综述,专门阐述了在应用药效学和药动学原理评估QNs的合理剂量时,必须根据游离药物浓度而不能以总的药物浓度来估算。
血液与组织中的游离药物浓度存在着某种平衡关系,因此通常血清中游离QNs的浓度可反映细胞外液,即大多数感染部位的药物浓度。然而,潜在的障碍因素可能会影响到药物向感染部位的扩散,从而导致血清中游离药物浓度与细菌的药物暴露量之间出现差异。这种障碍包括成形的脓肿、血-脑屏障、细菌的生物膜系统和炎性碎片等。另外,药物的组织分布是考察药物药动学特征的重要指标之一。
人们常常根据QNs的主要消除途径将其分为以下三类:①经肾脏消除的药物,如ENR、奥比沙星、OFL、替马沙星和LOM;②经肝脏消除的药物,如DIF、PEF;③还有通过肾脏和肝脏共同消除的药物,如MAR、DAN、NOR、CIP和ENO。不同的药物分子类型和动物品种将大大影响QNs通过肝脏代谢的程度,且药物对应的完全消除半衰期的范围较广。QNs的代谢途径包括葡萄糖醛酸结合反应(格帕沙星、司帕沙星和莫西沙星)、N-氧化反应和脱甲基反应(左旋氧氟沙星和司帕沙星)。药物代谢通常会涉及细胞色素P450系统。
药物经肠黏膜主动分泌也是QNs消除的一种机制。胆汁分泌也可引起肠内药物的富集。肠肝(再)循环可以延长机体内某种化合物残留时间。
各种QNs在肾脏的消除程度各异。左旋氧氟沙星和加替沙星主要通过肾脏来消除,其中肾脏中左旋氧氟沙星的清除率要比肌酐的清除率约高出60%。这一点表明其与肾小球滤过作用和肾小管部分都有关。服用一定剂量的丙磺舒或西咪替丁后可使某些QNs的肾清除率增加24%~35%。丙磺舒也可以延长加替沙星和CIP的完全消除半衰期。另外,钙、铁、镁、铝等离子能与QNs发生螯合,影响内服药物的吸收,降低生物利用度和血中浓度。
3 毒理学
QNs的毒性主要取决于药物剂量和动物种类。QNs的毒性在治疗剂量内是温和的,一般产生胃肠道的紊乱,如恶心、呕吐、腹泻;较高剂量时,出现眩晕、烦躁、头痛、嗜睡或无睡眠的中枢神经系统症状;高血浆浓度可以产生立即的毒性反应,可能由于过多的组胺释放所致。在医学上,已经报道的副作用有光毒性反应(尤其是PEF,而NOR和CIP很少发生)、药物之间相互作用、中枢神经系统的影响(包括癫痫、共济失调、眩晕、失眠、疲倦、嗜睡和震颤)以及结晶尿(引起尿路梗阻)。在犬、猫中也有关于这些副作用的报道。此外,兽医治疗中毒性反应还包括胃肠道代谢紊乱,如反胃(恶心)、呕吐和腹泻,幼畜关节病(特别是犬),以及对眼的毒性(包括猫视网膜变性和由某些QNs引起的囊下白内障)。
另外,由于QNs作用机制的因素可能具有致癌或遗传毒性,研究人员已证明ENR在实验动物中显示一定的致突变和胚胎毒作用,OXO、NAL对大鼠有潜在的致癌作用。QNs与其他药物之间相互作用的不良反应也不容忽视,在进行QNs的联合应用时要谨慎。
因而,动物源性食品中残留的QNs除对动物本身造成损害外,还可以通过食物链进一步对人体产生更大的危害。
4 耐药性
随着QNs的广泛应用,动物源性食品中残留较低浓度的QNs容易诱导人类致病菌产生耐药性,耐药性问题也是QNs是否被允许在畜牧养殖业中使用的争论中所关注的焦点。经过广泛研究发现,QNs的耐药性主要是由于细菌DNA促旋酶(拓扑异构酶Ⅱ)的靶基因突变而引起的,而拓扑异构酶Ⅳ的次级突变将导致更高水平的耐药。可导致细菌耐药的氨基酸取代基目前已定位在(或局限在)gyrA和parC基因部的特定的拓扑异构酶亚区(称为喹诺酮耐药决定区,QRDR)。
在选择性的压力下QNs的细菌耐药性可经克隆广泛地传播。目前,研究者首先在临床分离的肺炎克雷伯氏菌中发现了一种质粒介导的喹诺酮耐药基因(qnr),后来又在大肠杆菌中发现。这一基因位于邻近Ⅰ类整合子的序列(qacEA1,sulI),qnr基因编码一个由218个氨基酸组成的蛋白质,此蛋白质属于五肽重复族。对于浓度依赖性抗菌药物,qnr通过保护DNA促旋酶(而不是拓扑异构酶Ⅳ)免受CIP的抑制来发挥其作用。qnr基因使细菌对喹诺酮敏感性稍稍降低,以致在临床认为qnr+株仍然是敏感菌。
每一种喹诺酮耐药机制(作用靶位的改变、通透性降低、外排泵作用以及靶位受到保护)都可同时存在于一个细菌中,进而导致更高水平的耐药性。到目前为止,还没有发现基于酶的失活或变性的喹诺酮耐药机制。由于喹诺酮为合成抗菌药物,没有天然类似物,因此形成这种耐药机制的可能性很小。
5 国内外限量要求
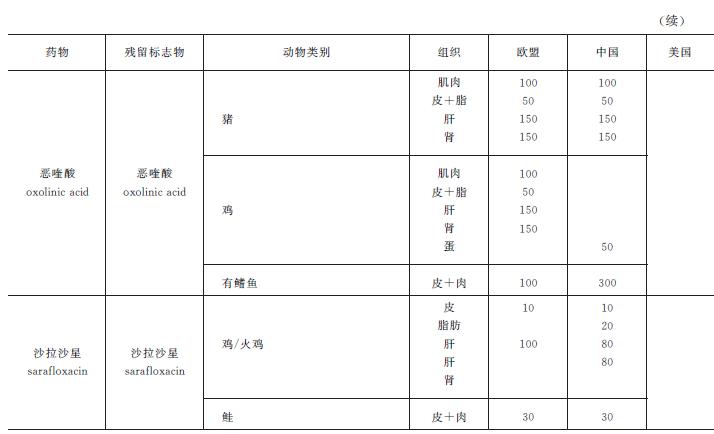
由于QNs在医学临床上也是一类十分重要的抗感染药物,目前QNs残留最受关注的危害是动物的耐药菌株特别是肠道细菌通过食物链向人类传播。为了保护消费者的健康安全,中国、欧盟、美国等都已制定QNs在各动物组织中的MRL,如表5-18所示。因弯曲杆菌耐QNs菌株的出现,美国FDA于2005年已禁止ENR作为饲料添加剂用于禽类饲喂。日本也于2006年5月29日开始实行了更为严格的“肯定列表制度”,在原有制定有MRL的药物基础之上,还将原来未规定MRL的药物的MRL一律定为10ng/g。2015年9月1日,我国农业部发布第2292号公告,明确禁止洛美沙星、培氟沙星、氧氟沙星、诺氟沙星等4种氟喹诺酮类抗菌药用于食品动物生产中。



6 QNs残留的分析方法
由于QNs在临床上的应用越来越广泛,QNs的残留分析方法也受到了较大的关注,有关分析方法的报道也日益增多,近年来,已有多篇综述专门讨论了QNs的分析方法。
QNs残留分析通常包括:选用适当的溶剂提取,进一步利用液-液萃取、固相萃取等进行净化、浓缩,最后用高效液相色谱法(HPLC)、高效毛细管电泳(CE)、液相色谱质谱联用技术(LC-MS)等方法进行检测,有时还使用气相色谱法(GC)、高效薄层色谱法(HPTLC)、微生物法(MA)、免疫分析法(IA)等进行测定。
6.1 样品前处理方法
6.1.1 提取方法
QNs属于强极性化合物,且在3位上都有羧基而具有酸性,在7位上有哌嗪基的喹诺酮含有氨基而具有碱性,因此在水溶液中,哌嗪喹诺酮有3种离子形态(阴离子、两性离子、阳离子),而其他喹诺酮则只有2种形式(阴离子或中性分子)。QNs的结构决定了其可溶于极性有机溶剂、水不溶性有机溶剂或酸性、碱性水溶液中。因此可以通过多种途径从生物基质中提取QNs,主要的方法包括:①用强极性有机溶剂提取,如*酮丙**、*腈乙**、乙醇或甲醇;②用缓冲溶液和水不溶性有机溶剂进行提取,如乙酸乙酯、三氯甲烷或二氯甲烷;③用酸性水溶性有机溶剂或碱性水溶性有机溶剂,如磷酸-*腈乙**、乙酸-*腈乙**、三氯乙酸-*腈乙**、*水氨**-*腈乙**、乙酸-甲醇、三氯乙酸-甲醇、*腈乙**-水溶液、高氯酸-磷酸-甲醇、三氯乙酸溶液;④用水溶液提取,如磷酸水溶液、盐酸溶液、磷酸缓冲溶液、氢氧化钠溶液等。
(1)水不溶性有机溶剂提取 早期QNs残留分析方法常用乙酸乙酯、三氯甲烷、二氯甲烷等水不溶性有机溶剂进行提取。乙酸乙酯适用于多种生物样品基质的提取,更适用于疏水的酸性QNs(如OXO、FLU等)。QNs可以用乙酸乙酯、三氯甲烷、二氯甲烷等以无水的溶液从组织样品中提取,也可同时加入一定缓冲液进行提取。由于QNs系酸碱两*药性**物,在提取过程中,常考察无水硫酸钠的加入量对提取效率的影响,以提高乙酸乙酯的提取效率,结果表明,无水硫酸钠对待测物回收率有重要影响,5mL样品中加入4g无水硫酸钠时,乙酸乙酯的提取效率最高。利用该方法进行提取时通常将样品与乙酸乙酯混合或振荡,而且在多数情况下,需要使用20~50mL的乙酸乙酯,有时达100mL。
用三氯甲烷和二氯甲烷来提取生物样品基质中的二氯甲烷-QNs残留时,可以直接浸提,也可用缓冲液与三氯甲烷或二氯甲烷合并进行液-液萃取,还有报道用甲醇进行的索氏提取。用二氯甲烷索氏提取法可获得较高的回收率,但处理过程复杂、费时,并需要大量的有机溶剂。与之相比,用pH7.4缓冲液和二氯甲烷更加简便和快速,这种方法虽然回收率较低,但较适用于大批样品的常规检测。
(2)水溶性有机溶剂 *酮丙**、*腈乙**、甲醇、三氯乙酸、高氯酸、*腈乙**-四氢呋喃(THF)混合物等水溶性有机溶剂也常被用来作为提取组织样品中QNs的溶剂。与乙酸乙酯相似,*酮丙**也主要被用来提取NAL、OXO、PIR、FLU等酸性喹诺酮类药物(acidicquinolones,AQNs),*腈乙**、甲醇及酸化*腈乙**-甲醇、碱化*腈乙**-甲醇等已被广泛用于NOR、ENR、CIP、DAN、SAR等两性喹诺酮类药物或哌嗪基喹诺酮类药物(piperazinyl quinolones,PQNs)的提取。研究者还发现,使用酸化或碱化的*腈乙**-甲醇提取ENR、CIP等PQNs时,较使用单纯有机溶剂的效果要强,提取杂质少,回收率高。在分析AQNs时,使用*酮丙**提取,其回收率要比使用*腈乙**高。
此外,*腈乙**-水的等量混合溶剂对SAR具有显著的“潜溶(cosolvency)”效应,溶解度增至4mg/mL以上,即可有效提高方法的回收率。Bauer、Meinertz等研究发现,使用*腈乙**-水(1∶1)提取鱼饲料和鲶组织中的SAR及其他PQs时,*腈乙**-水不但可以有效溶解和提取SAR,而且提取的杂质较少。
(3)酸性或碱性有机溶剂 由于QNs在甲醇、*醚乙**、氯仿等有机溶剂中的溶解度较低,而易溶于稀酸或稀碱中,所以酸性或碱性的溶液更适合作为组织样品中QNs的提取溶液。最常用的提取液包括盐酸、三氯乙酸、高氯酸-磷酸的水溶液,及其与甲醇、*腈乙**的混合溶液。三氯乙酸-*腈乙**、*腈乙**-氢氧化钠溶液、*腈乙**-*水氨**溶液、乙酸-甲醇等酸化或碱化的有机溶剂对QNs尤其是FQs具有较强的提取效率,因为这些溶剂对QNs具有较高的溶解性,并兼有良好的组织渗透性、脱蛋白质和释放药物的作用。Volmer、Tyczkowska等研究发现,使用碱化溶剂处理奶样品时,碱化溶剂有助于药物的释放。
Roybal等专门研究了甲醇、乙醇、*酮丙**、二氯甲烷等对组织中SAR、DAN、ENR和CIP等QNs的提取效率。试验发现,使用酸化的甲醇或酸化的*酮丙**(pH3.0)较单一或混合的纯有机溶剂,能有效改善提取效率,回收率可达70%~90%,可能是在酸性条件下,质子化的QNs与样品基质的吸附作用减弱的缘故,利于药物的释放。QNs为酸碱两性物质,介质中水分含量约1%时,对QNs的解离状态具有调节作用,并考察了无水硫酸钠的加入量对提取效率的影响,结果表明无水硫酸钠对待测物回收率有重要影响,5mL样品中加入4g无水硫酸钠时提取效率最高。
在组织样品提取过程中,通常采用振荡等操作来完成,有时也使用超声、均质等方法。且多数的提取需重复两次进行,使用的提取溶剂为5~100mL。
(4)缓冲溶液 在分析QNs时,还经常使用中性磷酸盐缓冲液,或使用偏磷酸、磷酸、盐酸、氢氧化钠等酸碱水溶液作为提取溶剂。大多数的碱性溶液几乎专门(仅)用于AQNs的提取,然而PQNs最好用pH接近于7的溶液来提取。在某些情况下,可在提取的同时用正己烷或乙二醚-正己烷的混合物进一步脱脂。
手动振荡通常可达到提取平衡,也可使用超声处理。所需样品的量为0.5~10g,所需提取液的体积为1~50mL。
6.1.2 净化方法
由于样品基质性质复杂,样品提取过程中会有一些与待测组分性质类似的共萃取物一起被提取出来,这些杂质常常干扰光谱检测、增加基线噪声、降低柱效、阻塞色谱管路、污染色谱柱和检测器等,因此在色谱等检测之前进行净化操作是必不可少的。净化处理方法主要包括液-液萃取(LLE)和固相萃取(SPE)两大类。
酸、碱LLE是净化QNs的基本方法。这种方法是通过调节水相的pH使得待测物由其中一相转移到另一相,从而实现样品净化。氯仿、二氯甲烷、乙酸乙酯等常用作液-液分配的溶剂,有时还可加入氯化钠等以增强溶剂的离子强度进一步提高QNs在有机相中的转移效率。另外,将样品基质提取后,通常会用正己烷、*醚乙**等非极性溶剂进行脱脂。由于LLE过程中需要使用大量的有机溶剂,尤其是二氯甲烷、氯仿等氯制剂,而且操作步骤繁琐,现在LLE方法已逐步被SPE所代替。
SPE净化方法主要用于极性溶剂提取组织样品中QNs之后。在SPE净化前,通常还根据试验需要用正己烷进行脱脂。SPE主要包括硅胶基C18填料、DiscoveryDSCC18、聚乙烯-苯乙烯-二乙烯基苯(PSDVB、ENV+、SBD-RPS、HLB、StrataX等)、离子交换柱(SCX、PRS、MPC)等,这些填料都被用于QNs的净化。
由于QNs为酸碱两性物质,故SPE固相基质对QNs的保留主要依靠样品载液的pH。Golet等将样品溶液pH调节为3.0,用MPCSPE柱净化,回收率达80%以上。Ferdig等专门比较了3种不同的聚合SPE柱Oasis HLB、Isolute ENV+、LichrolutEN+和3种不同的硅胶基反相柱Chromabond C8、Chromabond Tetracycline、Bakerbond phenyl的保留、净化效果,结果发现,以上6种SPE柱对两性QNs均能有很好的回收率,而对AQNs如OXO、FLU的回收率较差。
随着科学技术的发展和兽药残留检测要求的不断提高,各种新技术、新手段也被用来作为生物样品中QNs的样品前处理方法,主要包括基质固相分散(MSPD)、超临界流体萃取法(SFE)、固相微萃取(SPME)、微波辅助萃取(MAE)、加速溶剂萃取(ASE)、分子印迹固相萃取(MISPE)、自动序列透析/痕量富集(ASTED)、超滤透析等。
6.2 检测方法
国内外对QNs残留检测技术的文献报道很多。目前用于QNs残留检测的方法主要有高效液相色谱HPLC)、毛细管电泳(CE)、液相色谱-质谱联用(LC-MS)、ELISA等,仅有少数报道用气相色谱(GC)、高效薄层色谱(HPTLC)、微生物法等检测QNs的残留。
6.2.1 LC
分离通常使用硅质反相色谱柱,其中主要为C18/C8固定相,但在有些情况下也引入苯基或氨基键合的固定相。由于色谱柱填料残留硅醇基(硅羟基)和金属杂质,因而普通的反相柱导致严重的色谱峰拖尾。因此多数方法使用经端基封闭处理的色谱柱或高纯硅质柱,如Inertsil、Kromasil、Puresil、Versapack、Wakosil、L-column、LUNAor ZorbaxRX等,这些柱子几乎不含痕量金属离子。
使用PSDVB聚合物色谱柱对QNs进行分离是另一种避免拖尾峰的途径。然而,这些色谱柱的效率要低于硅质柱,由于FQs结构上的哌嗪基垂直连于喹诺酮环上,而固定相中的苯基易与哌嗪基之间形成空间位阻,因此PQNs几乎不能保留在这些色谱柱上,因此PSDVB聚合物色谱柱更适合于FLU和OXO等AQNs的分离检测,在某些情况下也用于ENR、CIP和SAR的分析。离子交换色谱法也可用于NAL的测定。
分析QNs的流动相组成主要是*腈乙**-水二元溶剂体系,有时也使用*腈乙**-甲醇-水、*腈乙**-四氢呋喃-水或*腈乙**-二甲胺-水等三元溶剂体系,也有报道使用*腈乙**-甲醇-四氢呋喃-水四元溶剂体系。少数论文报道有使用不含*腈乙**的流动相,同时这些流动相由甲醇-水构成,且甲醇所占的比例高于30%。梯度洗脱方法常被用于极性差异较大的QNs多残留分析。
为了改善峰形可在这些流动相中加入一些扫尾剂,这样可以减少硅醇基的电离,另外将流动相pH控制在2~4,能尽可能降低其与喹诺酮阳离子之间的相互影响。磷酸盐缓冲液、柠檬酸盐缓冲液、草酸缓冲液等经常被作为检测QNs的流动相用以调节pH,以获得较好的分离。在流动相中加入THF,也可以减少拖尾峰的出现。
QNs在酸性流动相条件下呈离子状态,故可在流动相中加入季铵盐、烷基硫酸钠或烷基磺酸钠等离子对试剂。如烷基硫酸钠或烷基磺酸钠可与质子化的待测物及三乙胺或季铵盐形成离子对,而三乙胺或季铵盐可与待测物竞争残留的活性硅醇基,能够获得更好的保留、洗脱和更大程度的分离效果。
由于多数的流动相不适用于质谱(MS),在LC与MS联用时应选用挥发性的添加剂。因此可采用乙酸胺或甲酸胺、乙酸和三氟乙酸与*腈乙**组成流动相体系,以获得更强的灵敏度、更好的稳定性。
QNs具有较强的紫外吸收和荧光性质,特别是FQs的光谱性质很相似,为设计多残留分析检测方法提供了条件。早期研究通常使用UV进行检测,由于FLD较UV灵敏度可提高2~3个数量级,近年来已广泛使用检测更灵敏、选择性更强的FLD测定QNs在生物样品中的残留。QNs有两个吸收波段:第一个为宽波段(300~350nm),所有的喹诺酮类化合物(药物)的宽波段都是完全相同的,而第二个波段位于245~290nm,每种喹诺酮在此波段都具有特异性。其在第二波段的吸光度要比第一波段高,因此通常选择第二波段来检测。然而,在某些情况下为了减少样品基质的干扰和基线噪声,可选用325~330nm波长进行检测。
PQNs与AQNs的荧光光谱有较大差异,一般PQNs的激发光谱范围是275~280nm、发射光谱范围是365~450nm,而AQNs的激发光谱范围为325nm、发射光谱范围是350~400nm。与UV吸收不同,荧光性主要取决于其介质的pH。QNs为阴离子状态时,一般没有天然荧光,而在低pH(2.5~4.5)条件下可获得最强荧光。在这个pH范围内,AQNs和PQNs的中性和阳离子类型占优势,而且pH在2~4的流动相对QNs的分离也是最佳的。AQNs的激发和发射波长分别设定在325nm左右和360nm左右,虽然在某些情况下激发波长也设定在光谱第一波段。对PQNs来说,其激发和发射波长分别设定在275~280nm和440~450nm。PIR和MAR的自身荧光较弱,多采用UV检测法来测定。
在使用荧光检测法进行QNs多残留检测时,采用程序波长检测法,可使每种分析物的检测波长处于其自身波长范围内(可检测出每种分析物的自身波长),以提高检测灵敏度和选择性。程序波长检测法也被用于某些基质中哌嗪基喹诺酮类药物(PQNs)或者AQNs和PQNs混合物的荧光测定。在色谱分析中将UV和FLD串联使用可实现荧光性喹诺酮和非荧光性喹诺酮的同步检测。
6.2.2 HPCE
CE与HPLC一样属于液相分离技术,已成为一种与HPLC相互补充的分离分析方法。QNs由于结构上的相似而表现出相似的物理化学性质,采用CE同时测定多种QNs具有一定的难度。Fierens等采用区带电泳分离方法,利用磷酸盐缓冲溶液为分离缓冲体系,检测了OFL、PEF、NOR、CIP、ENR、OXO、NAL、吡哌酸、西诺沙星、氟罗沙星10种QNs。
Hernández、Awadallah、Schmitt-Kopplin、Ferdig等分别建立了检测QNs的CE。Barbosa等利用CE、HPLC、电位测定法和分光光度计法比较分析了两*药性**物(含QNs)在甲醇-水溶剂体系中的pKa。Barrón用SPE净化、CE检测了鸡组织中OXO与FLU的残留、ENR与其代谢产物CIP在生物样品中的残留。McCourt等建立了FQs多残留的毛细管区带电泳-ESI-MS/MS方法;Lara等建立了检测牛奶中QNs多残留的CE-ESI-MS/MS方法。
6.2.3 GC
由于QNs是强极性化合物,必须在GC分析之前生成挥发性的衍生物,因此仅有少数论文报道了QNs的GC方法,而且主要是在20世纪80年代所报道的。由于样品衍生化采用酯化反应时容易生成强极性化合物,所以QNs的衍生化方法通常使用还原-脱羧衍生化方法(NaBH4法)。Takatsumki建立了检测鱼组织中OXO、NAL、PIR的GC-MS方法,该方法利用DB-S硅基柱,以氢气为载气,待测物用NaBH4法后进行检测。Wang等利用衍生化GC测定了西诺沙星。
6.2.4 HPTLC
周源等以聚酰胺层析板为固定相,以0.01mol/L的十二烷基磺酸钠和0.05mol/L的EDTA混合水溶液为展开剂,建立了胶束HPTLC检测了体液中NOR和氟罗沙星的含量。Juhel-Gaugain等建立了检测猪肉中NOR、CIP、DAN、ENR、OXO、FLU、NAL7种QNs的HPTLC快速分析方法,样品经提取净化后,利用硅胶-60为固定相、甲醇-*水氨**为展开剂,展板晾干后在312nm处检测,QNs呈淡蓝色荧光斑,OXO和FLU不显色,喷以荧光增强剂-氯化铽溶液,100℃加热5min,312nm处检视,OXO和FLU呈淡黄色荧光斑,方法的检测限低于15ng/g。
6.2.5 LC-MS
用紫外吸收或荧光检测法进行检测,仅能得到样品的光学信息,无法对样品进行确证。目前主要采用质谱检测器作为确证方法。质谱检测器与FLD不同,属于通用型检测器,LC-MS检测方法包括单纯确证方法和确证同时定量的检测方法。早期的液质联机检测主要是检测单一药物和单纯确证方法。
为了提供更高的选择性,首选涉及特殊*能官**团的裂解途径。有几种接口已被用于LC-MS(或LC-MS/MS),而且总是在正离子模式下。热喷雾法最初是用于鱼肉中AQNs的分析,由于它是一种较温和的电离技术,所以只能获得[M+H]+所对应的峰。
大气压化学电离接口已被用于具有源内碰撞诱导解离(collision-induceddissociation,CID)技术的LC-MS和LC-MS/MS。对PQNs来说,在低CID电压条件下只能观察到[M+H]+和[M+H-H2O]+及它们的同位素所对应的峰。对AQNs来说,在低锥体电压下获得的质谱图中包括[M+H]+、[M+Na]+和[M+H-CO2]+,在高锥体电压下还会显示出[M+H-H2O]+所对应的峰。
在确证分析QNs时,更多采用的是电喷雾电离(ESI)介导的LC-MS(MS/MS)。LC-ESI-MS是近年来发展最快的LC-MS,ESI既是接口,又是离子源,是一种大气压下的软电离技术,特别适用于QNs等极性分子的汽化和离子化,可以得到待测物分子的正离子峰,通过调节锥体电压,实现源内诱导碰撞解离或MRM,可获得足够的待测物结构信息,如2~3个稳定的具有特征性的碎片离子。Schilling等报道了鲶组织中SAR的LC-ESI-MS/MS确证方法,详细讨论了作为一种联用或多维分析确证残留组分的原则和方法;主要通过调节碰撞室电压优化MS/MS测定条件,利用源内碰撞质谱电离进一步确定SAR的裂解途径,m/z386[M+H]+为准分子离子峰,结合保留时间对确证SAR具有重要意义,[M+H-H2O]+、[M+H-CO2]+是与羧基有关的裂解产生的碎片,将上述3个离子峰作为监测离子,在MRM模式下进行确证分析。
Voimer等报道了多种QNs的LC-ESI-MS/MS多残留检测方法。文中讨论了QNs的结构、理化性质、流动相pH对色谱分离、保留值和ESI的影响,以及QNs的裂解途径和各种MS/MS分析模式在QNs残留分析和代谢中的应用。
6.2.6 免疫分析方法
HPLC、CE等色谱方法虽然能取得很好的试验结果,但是需要复杂的前处理过程和昂贵的仪器。免疫分析方法以抗原抗体的特异性反应为基础,具有高特异性、高灵敏度的特点,可使分析过程简化,适合复杂基质中痕量组分的分析。免疫分析可分为两大类:一类为相对独立的分析方法,即免疫测定法,如ELISA、荧光免疫测定法、免疫胶体金技术、免疫传感器等,另一类是将免疫分析技术与理化分析仪器联用,较为常见的是免疫分析技术与HPLC的联用。在联用方法中,免疫分析技术可作为HPLC等测定技术的样品分离净化手段。
QNs结构中含有羧基,故多采用羧基与载体蛋白游离氨基进行反应,将QNs与载体连接合成人工抗原,进而免疫动物,使动物产生特异性抗体。由于QNs的主要结构部分相同或相似,因此某一QNs的抗体通常对其他QNs存在一定的交叉反应。
Sintkoff等建立了检测CIP的间接竞争ELISA,用NHS-EDC法将CIP与钥孔血蓝蛋白(KLH)和牛血清白蛋白(BSA)连接制备免疫抗原和包被抗原,用KLH-CIP免疫新西兰白兔,制备抗血清,用BSA-CIP做包被抗原,建立标准工作曲线并检测CIP。Bucknall等制备了NOR的抗体,检测了牛奶、羊肾脏中NOR、ENR等10种QNs的残留。Huet等制备的SAR单克隆抗体对SAR、NOR、FLU等15种QNs都有交叉反应性,鸡肌肉、鸡蛋、肾脏等组织经甲醇磷酸盐提取后,用建立的ELISA进行检测,检测限为10~200ng/g。Lu等利用PEF的抗体借助ELISA检测了鸡肝脏中残留的PEF,平均回收率为86%~106%。Coillie等利用制备的FLU人工抗原免疫产蛋鸡,收集鸡蛋并对IgY进行分离、鉴定,用建好的间接竞争ELISA测定了牛奶中的FLU。Holtzapple等制备了SAR的单克隆抗体和多克隆抗体,使用分子力学和量子力学的方法获得了三维分子模型,并讨论了交叉反应与结构的关系和不同结构部分对免疫结合反应的作用,使得对待测物与抗体的结合有了更好的理解,由此也说明利用计算机和分子模型技术设计半抗原和预测抗体选择性是可行的。蔡勤仁等制备了ENR的单克隆抗体,并建立了Ci-ELISA,其检测限为0.13ng/mL,与CIP、MAR、SAR、DAN的交叉反应率分别为111%、27%、71%和37%,与头孢氨苄、氯霉素和SDM无交叉反应。
Mellgren等研制了能检测牛奶中ENR及其代谢物CIP的表面等离子共振(surface plasmon resonance,SPR)免疫传感器,其探头表面覆盖着可更换的固定有ENR的传感膜,当固定ENR与制备的抗体发生结合反应时,引起探头表面折射系数变化,同时折射角发生位移,借此对样品中待测物进行测定。
Holtzapple等还建立了高效免疫亲和色谱法(HPIAC)检测牛奶、血清、鸡肝脏中CIP、ENR、SAR和DIF的残留。