近年来,化石能源的消耗量日益增多,不可再生能源的储量也开始减少,同时CO2大量的排放,造成的温室效应等环境问题也日日突出。因此,就如何减少CO2排放量,以及如何对已排放的CO2进行回收、固定、再资源化利用等问题,已引起了世界各国学者的广泛关注。
目前,人们提出的降低大气中CO2含量的方法主要围绕两大主题:一是CO2的捕集封存;二是CO2的转化利用。前者需要额外的能量消耗,而且生态安全性也存在一定隐患; 而后者则是一种通过化学或光、电催化还原方法,使大气中的CO2转化为可利用有机物的理想模式。
特别是光催化还原,它不需要外加电能或热能,在光催化剂存在下,可直接利用太阳能,在常温常压下将CO2还原成碳氢化合物,被认为是最理想的CO2处理技术
经各国学者的共同努力,目前已有一系列用于光催化还原CO2的光催化材料问世, 特别是其中的金属氧化物半导体,因优良的光催化活性而得到了广泛研究。
由研究结果看,二氧化钛(TiO2),,氧化锌(ZnO)等的带隙宽度较大(TiO2的带隙宽度大约3.17eV,ZnO的带隙宽度为3.2eV),通常在紫外光下才有催化活性,对太阳光的利用率很低;而氧化亚铜(Cu2O)是一种典型的金属缺位P型半导体,带隙宽度在2.0-2.2eV之间,是一种可在可见光范围内使用的理想光催化剂,而且具有成本低廉,制备方法简便及环境友好等优点。

但遗憾的是Cu2O具有光生电子-空穴对容易复合的缺陷,这会导致其光催化效率低,另外,Cu2O纳米粒子在应用过程中很容易因团聚而失活, 而且又因为分散在水体中,其回收再利用也有一定困难,需要寻找合适的方法来解决。
纤维素是地球上最为丰富的天然高分子,不仅具有良好的生物相容性和可自然降解性,而且还可通过其大分子基团的配位或电荷作用,引导纳米金属晶体在其表面聚集及生长,是良好的半导体光催化剂载体材料。
如果能通过氨基化处理或杂元素掺杂(尤其是氮和硫元素)等手段对纤维素进行改性后作为载体,它不仅能防止金属半导体氧化物纳米粒子的团聚,而且还有望依靠其表面特性,弥补Cu2O的光生电子-空穴对容易复合的不足,同时, 还因为纤维素的三维多孔结构,可吸附更多的CO2,提高复合催化剂光催化还原CO2的效率。
鉴于此,本论文以微晶纤维素为原料,通过混酸/超声结合法制得23.80±0.33nm粒径的NCC,并通过SOCl2氯化及EDA钝化等方法对其进行表面修饰,制得具有较高荧光量子产率的氨基化纤维素NCC-EDA后,利用NCC-EDA表面的氨基,羟基等*能官**团的配位及分散作用。
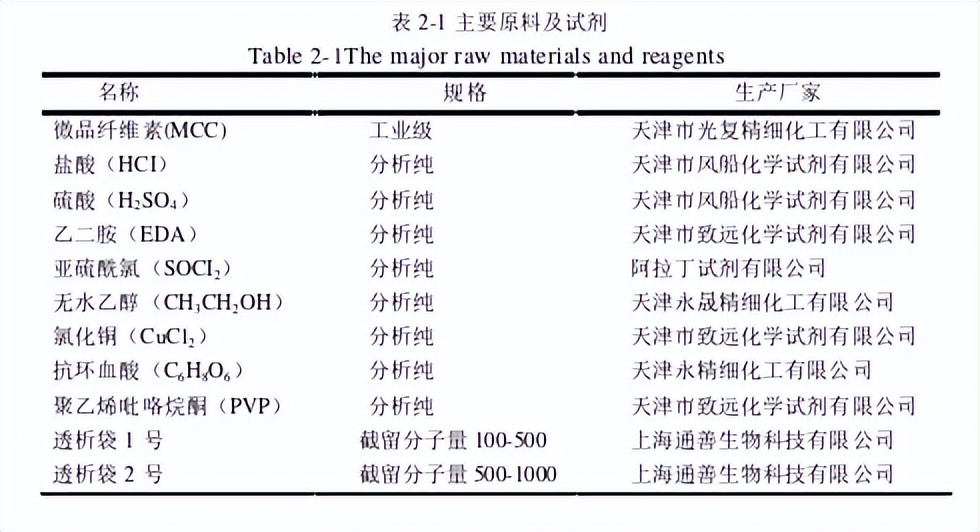
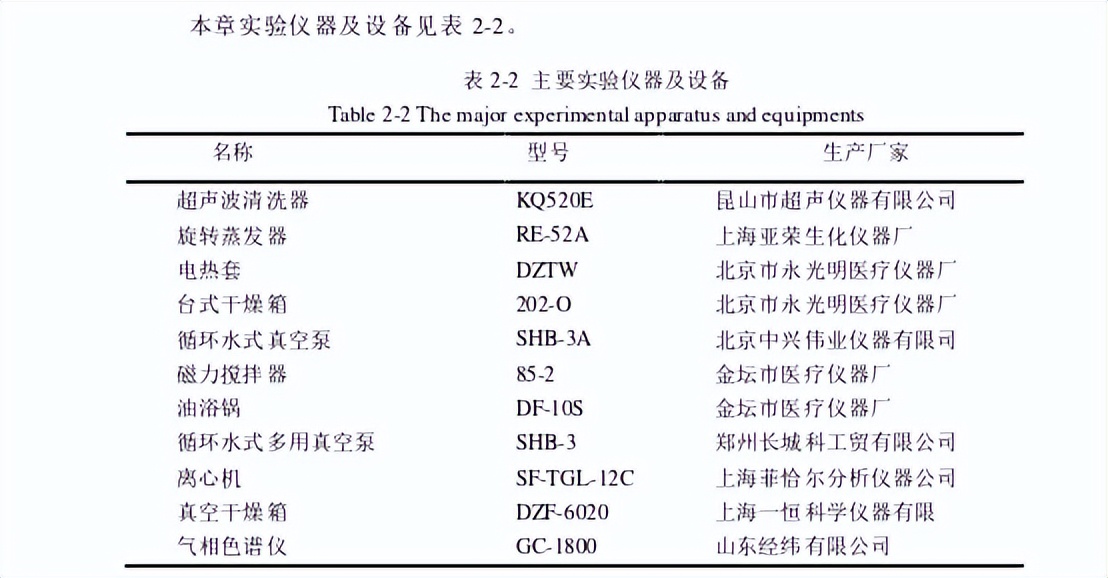
将由CuCl2•2H2O原位还原而得的Cu2O纳米粒子包覆于其中,制备了一种具有较高催化活性的复合光催化剂Cu2O/NCC-EDA,并在表征结构及光学性能的同时,考察了Cu2O/NCC-EDA的可见光催化还原CO2制备CH3OH的性能。本章实验所用试剂见表2-1。
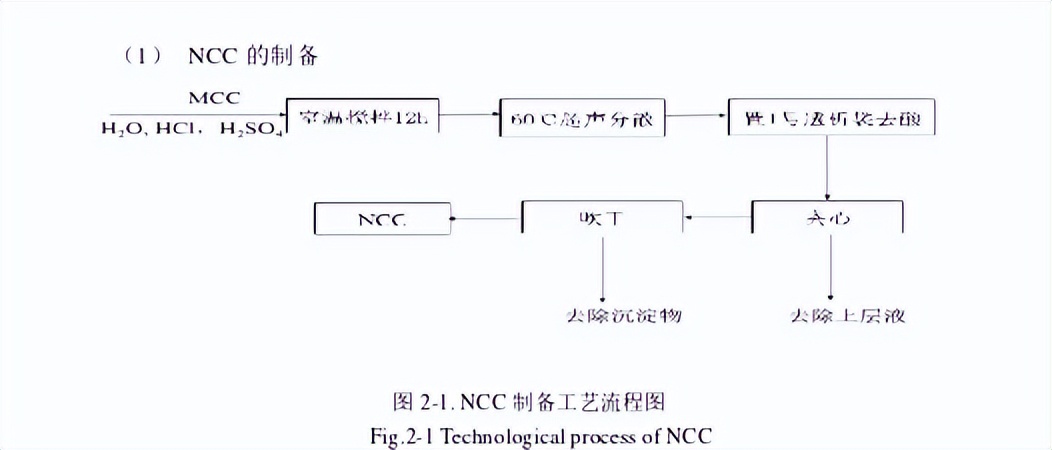
纳米纤维素晶体NCC的制备按照图2-1所示的步骤进行:按文献提出的方法制备NCC:取5gMCC于200mL广口瓶中,加入72mL去离子水,36mLH2SO4和12mLHCl,室温搅拌12小时后,60℃下超声分散12h,然后置入1号透析袋,在水中透析72h(期间不断换水)至PH=7后,将反应液移至离心管中进行离心分离(1000rpm,10min),取上清液得NCC的水分散体,将其吹干,得乳白色NCC产品。
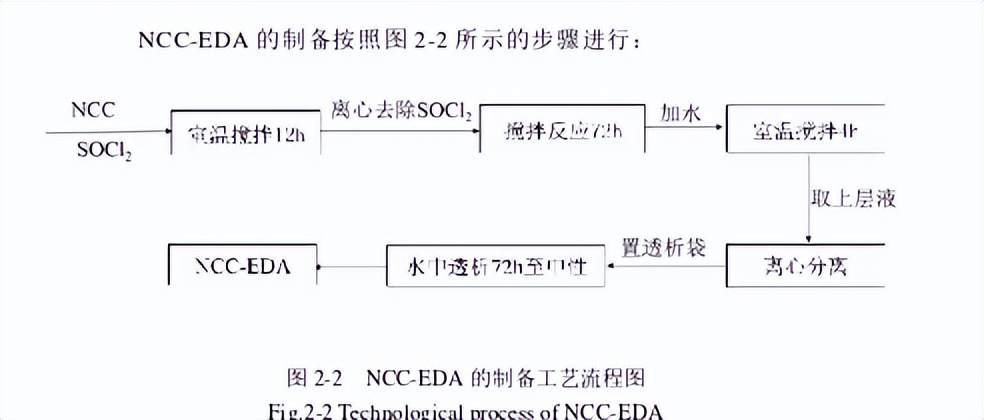
取1gNCC于反应瓶中,加入20mlDMF,室温下超声分散2h,使NCC完全分散成乳液后,加入SOCl2,50℃下搅拌反应12h,离心除去DMF和未反应的SOCl2,再用THF洗涤2次,制得氯化中间体NCC-Cl后,与EDA混合,130℃下回流反应72h,然后降温至60℃,加入30mL蒸馏水,再搅拌3-4小时后停止,高速(10000rpm)离心10min,取上层清液置入2号透析袋中(500-1000),在水中透析72h(期间不断换水),既得氨基化纤维素NCC-EDA的水分散体,减压蒸馏,得NCC-EDA颗粒。
通过改变NCC,SOCl2及EDA的比例,可获得具有不同N含量的产物。
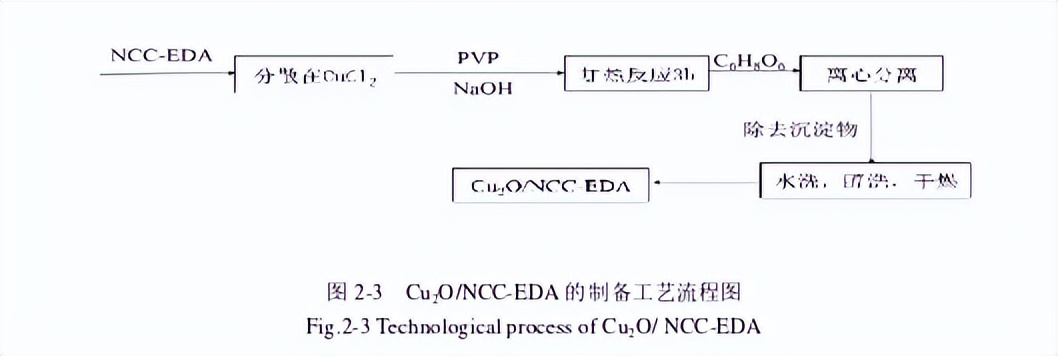
取25mLNCC-EDA水分散体,超声分散在25mL0.02mol/L的CuCl2水溶液中,得到均匀分散的浅蓝色乳液后,将其置入反应瓶中,搅拌条件下加入4.44gPVP,室温搅拌1h后升温至55℃,滴加5mL2.0mol/L的NaOH溶液,反应30min后,再加入0.6gC6H8O6,在55℃下恒温搅拌反应3h后停止,离心分离出沉淀物(10000rpm)。
通过水洗、醇洗、真空干燥(50℃)等步骤得橙黄色固体产物Cu2O/NCC-EDA。 通过改变NCC-EDA浓度,以及采用具有不同N含量的NCC-EDA,按上述试验方法可制备具有不同Cu2O含量,以及不同N含量的产物。


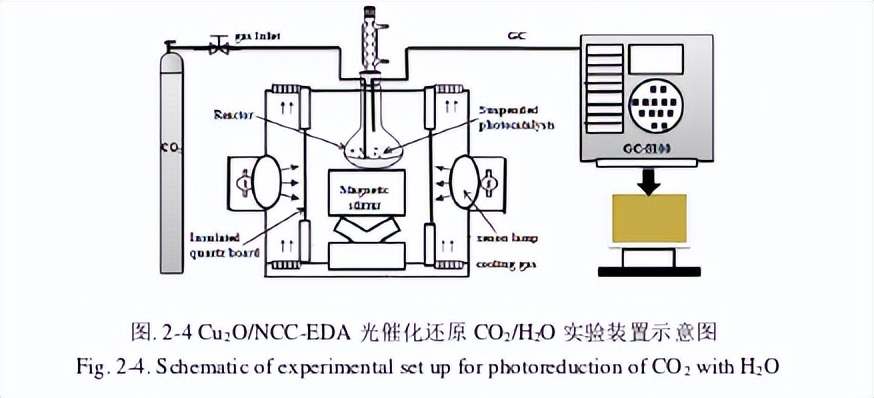
Cu2O/NCC-EDA光催化还原CO2实验在图2-4所示的自制光化学反应器中进行:取0.1g光催化剂和125ml0.5M的NaOH溶液于石英反应瓶中,然后超声溶解0.5h,移至如图2-4所示光催化还原反应装置中开启搅拌, 并持续通入CO2,其流量控制在200mL/min,黑暗吸收30min后打开光源(300W氙灯),进行光催化还原CO2/H2O的反应。
每隔2h用注射器取样,离心分离出清液,并用200nm滤膜过滤后,将样品注入气相色谱中,采用标准曲线法定量分析样品中的CH3OH含量。
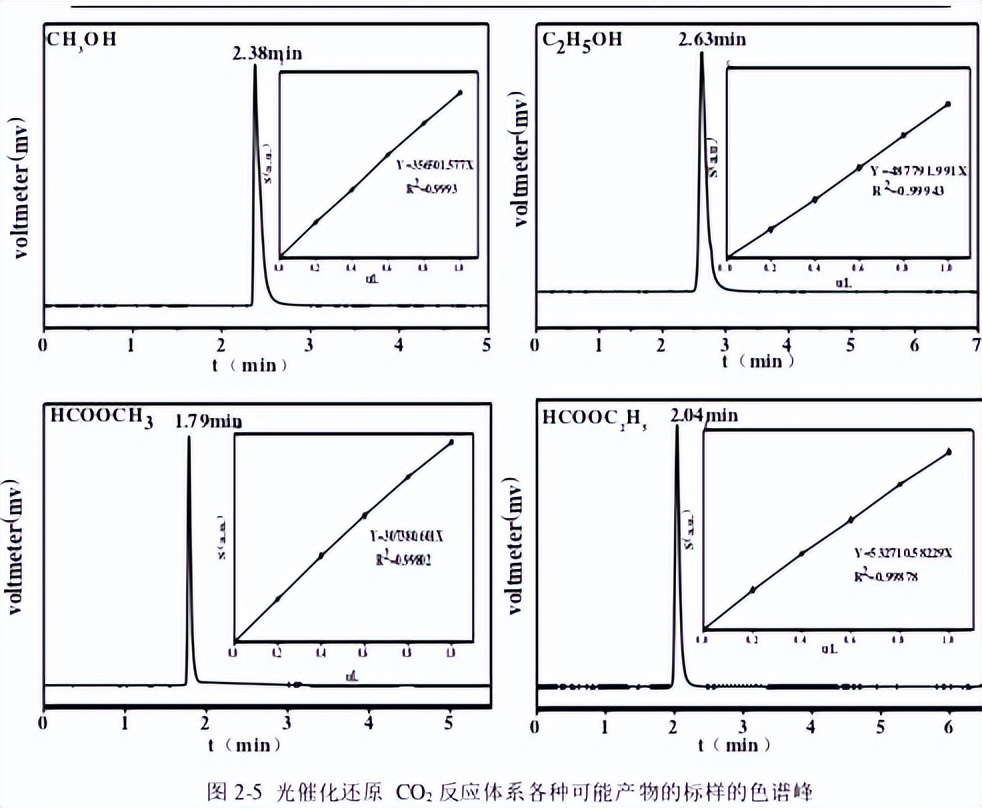
绘制液相CH3OH、C2H5OH、HCOOCH3及HCOOC2H5的标准曲线:采用色谱纯的CH3OH、C2H5OH、HCOOCH3及HCOOC2H5为标样,配置标准溶液,用进样器吸取0.2、0.4、0.6、0.8和1μL的标准液注入检测器中检测,记录CH3OH、C2H5OH、HCOOCH3、HCOOC2H5的停留时间和峰面积,进行反应产物的定性定量分析。将每个不同体积的标准液检测三次,其中停留时间基本不变,峰面积取三次平均值。 以体积为横轴,峰面积为纵轴绘制标准曲线。

(C)产物产量计算
(1)首先用气相色谱仪测得产物所对应的峰面积;
(2)再将数据代入对应停留时间物质的标准曲线谱的回归方程中,计算得到对应的浓度C1(μmol/ml)或体积V1(mL);
(3)液相产物产率=C1V1/m0,其中V1为反应液体积,m0为反应中加入的催化剂质量,计算可得液相产物产量(μmol·g-1cat);

由TEM可知本实验制备的NCC是粒径为23.80±0.33nm的球状颗粒,易团聚。 经EDA修饰后,氨基化纤维素纳米粒子NCC-EDA则是粒径分布在25-45nm之间的星形粒子(图.2-6a),是EDA链接在经SOCl2处理的而发生氧化及脱水碳化的NCC表面形成的,经氨基化处理,NCC-EDA不再团聚,均匀分散在水中。
由图2-6b看出,本实验制备的Cu2O呈立方晶型,边长约为80nm,分散性较差,极易团聚;而目的产物Cu2O/NCC-EDA(图2-6c)则是NCC-EDA链接在Cu2O表面,并将Cu2O包覆在其中形成的近球状颗粒,粒径约50nm,且具有树杈状凹凸不平的外壳,有利于吸附更多的CO2。
CC-EDA的存在,可能抑制了纳米Cu2O微晶的生-长,使包覆于其中的Cu2O尺寸变小,而且使产物表面变得粗糙,这有助于提高复合物比表面积及吸附反应物CO2/H2O的性能。

EDX测试结果表明,Cu2O/NCC-EDA主要包含有C,N,O,S及Cu五种元素(图2-6d),各元素含量分别为15.18%,4.40%,16.13%,0.29%及64.00%,说明Cu2O与NCC-EDA成功复合,Cu源自Cu2O,C和N来自NCC-EDA,而O则来自Cu2O及NCC-EDA。
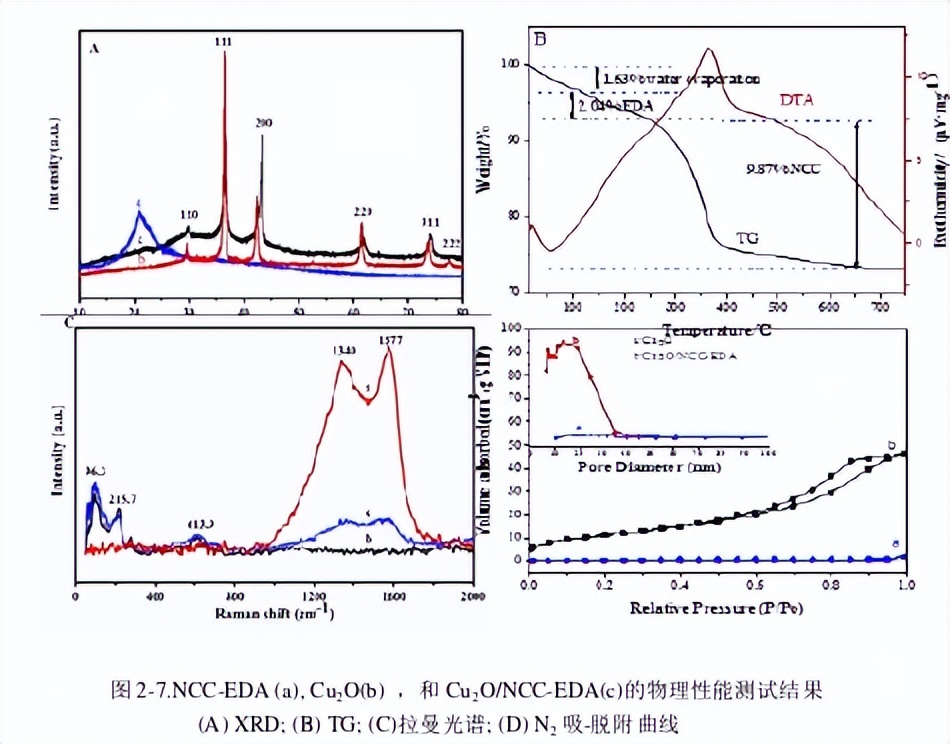
图2-7A展示了NCC-EDA(a)、Cu2O(b)及Cu2O/NCC-EDA(c)的XRD谱图。从图中可以看出,经SOCl2氯化及EDA钝化所得的产品NCC-EDA,因酸性试剂的渗透侵蚀,NCC的氧化及脱水碳化,Cl离子的引入及取代等过程, 除了代表纤维素002晶面的衍射峰降低之外,其他晶面的衍射峰完全消失,说明纤维素结晶度降低,结构在趋向石墨化。
Cu2O在2θ为29.51°,36.37°,42.31°,61.51°,73.64°和77.54°处出现了衍射峰,与立方晶相Cu2OJCPDS(No.05-0667)标准数据一致,分别对(110),(111),(200),(220),(311)和(222)晶面,没有出现Cu和CuO的衍射峰,表明所得产物是高纯度立方相Cu2O。Cu2O与NCC-EDA
复合后,产物中代表NCC-EDA的衍射峰右移,在15-50°范围内出现了对应石墨002晶面的较宽的鼓包峰,这可能是Cu2O的插入加速了NCC-EDA的进一步石墨化。
复合粒子Cu2O/NCC-EDA代表Cu2O的衍射峰基本与纯Cu2O相同,只是出峰位置稍向大角度方向移动,说明复合物中Cu2O的晶粒比较小,这点与TEM观察到的结果一致, 进一步说明NCC-EDA的包裹作用抑制了复合粒子中Cu2O的生长。
由图2-7B可以看出,Cu2O/NCC-EDA的大幅度失重分成三个阶段,第一阶段热重损失发生在100℃以前,为样品中水分的流失;第二阶段发生在107℃~204℃,这是由链接在纤维素表面的EDA基团热裂解造成的;第三阶段热重损失发生在245℃-600℃,为NCC的失重峰。
600℃以后还有86.56%未分解的残余物, 应该是结合在样品中的Cu2O。
由图2-7C展示的拉曼光谱可以看出,复合Cu2O/NCC-EDA于96.3,215.7和613.9cm-1处出现了三个对应纯Cu2O的拉曼峰,这进一步证明Cu2O存在于复合物中。
另外,NCC-EDA和Cu2O/NCC-EDA均在13681572cm-1处出现了分别对应石墨化结构的两个特征峰,既D峰和G峰,进一步表明NCC在SOCl2氯化及EDA钝化过程中,因氧化及脱水碳化等原因,使所得NCC-EDA的结构已趋向石墨化,作为载体,同石墨烯等材料一样,有望改善Cu2O光生电子-空穴对容易复合的缺陷。
对Cu2O及Cu2O/NCC-EDA进行N2吸-脱附实验,并采用BET方程计算样品比表面,采用BJH等效圆柱模型计算孔容大小及孔径分布,结果如图2-7D。
可以看出,Cu2O和NCC-EDA复合所得Cu2O/NCC-EDA的N2吸-脱附等温线曲线中有较大的滞后环,根据IUPAC分类,其等温线属于IV型等温线,是典型的介孔结构吸附脱附等温线, 说明复合产物中出现了介孔结构。
从孔径分布图(图.2-7D插图)中可以看出,孔径主要分布在6.2-34.9nm之间,较宽。其相应的BET比表面积,由纯Cu2O的13.57m2/g增加到了91.74m2/g,表明Cu2O与NCC-EDA的原位复合极大地提高了Cu2O的分散性与比表面积,这必将会改善催化剂吸附反应物的性能。
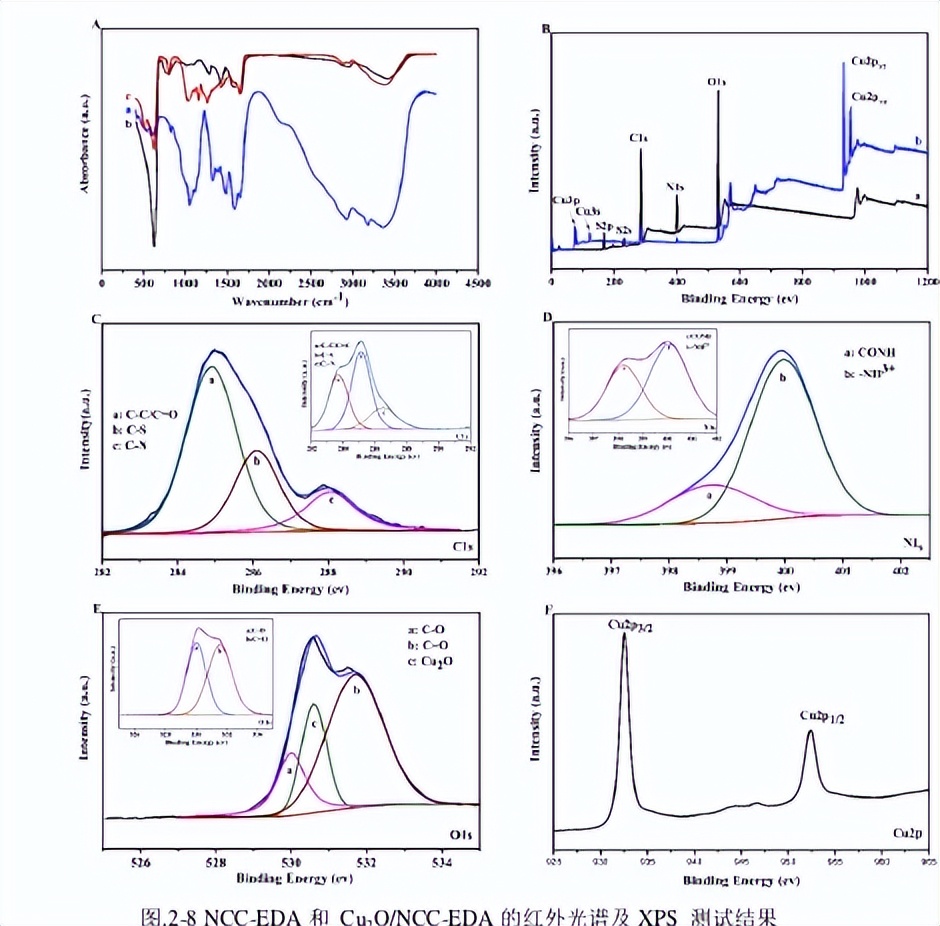
图2-8A展示的是(a)NCC-EDA、(b)Cu2O及(c)Cu2O/NCC-EDA的红外谱图。由曲线a可以看出,NCC经SOCl2氯化及EDA钝化后,产物NCC-EDA除了在3445及1058-1167cm-1处出现纤维素的特征峰之外,在3359和3184cm-1处出现了明显的酰胺基(CONH-)的特征峰;在1653,1585.2和1323.4cm-1处, 分别出现了酰胺Ⅰ带、酰胺Ⅱ带和酰胺Ⅲ带的吸收峰;在819及650cm-1处出现了代表O-S的特征吸收峰。
说明NCC已成功与EDA反应生成了氨基化产品NCC-EDA。反应过程中,因为NCC与SOCl2的氯化反应中间体未完全被EDA取代,所以NCC-EDA中含有少量S,这与EDX测试结果一致。由曲线b可知,Cu2O的特征吸收峰位于625cm-1处,与文献报道结果吻合。
位于3419cm-1处的吸收带表明Cu2O上吸附有羟基,可能来自Cu2O纳米颗粒表面吸附的水分子。 当Cu2O与NCC-EDA结合后,NCC-EDA位于3419cm-1处表示羟基的宽峰在产物中是向低频(3374cm-1)方向移动,且峰形变宽,这是因为NCC-EDA参与反应,其上的羟基与吸附于Cu2O上的水分子叠加,引起氢键作用的增强。
另外,NCC-EDA中位于3365cm-1和1582cm-1处的代表氨基的伸缩和弯曲振动的宽吸收峰在产物的FT-IR谱图中消失,这意味着NCC-EDA中的氨基参与其与Cu2O的复合作用。同时,产物FT-IR谱图中出现了代表Cu2O的新峰,且与纯Cu2O相比, 波数从625cm-1移动到了620cm-1处,强度减弱,这是NCC-EDA和Cu2O相互作用导致的结果。
X射线光电子能谱(XPS)可以用来分析纳米材料的组成及相应元素的化合价态。为了进一步确定产物Cu2O/NCC-EDA的化学结构以及其中铜的氧化态, 本论文也采用XPS分析了载体NCC-EDA和复合产物Cu2O/NCC-EDA。
图2-8B为NCC-EDA(a)和Cu2O/NCC-EDA(b)的XPS全谱。可以看出,NCC-EDA在531.0,399.8,285.0,231.7168.1eV处出现了五个特征峰,分别对应于O1s,N1s,C1s,S2S和S2p,表明NCC-EDA主要是由氧、氮、碳、硫四种元素成;Cu2O/NCC-EDA的XPS全谱中。
除了有对应NCC-EDA的O1s,N1s和C1s峰之外,多出了Cu3d,3p,3s,2p和CuAuger的峰,S2S和S2p峰消失,可能是复合物中增加了较高含量的Cu之后,S的相对含量较低,未在XPS谱图中显现出来。
参考文献:
- Hoffmann M R, Moss J A, Baum M M. Artificial photo-synthesis: Semiconductor photocatalytic fixation of CO2 to afford higher organic compounds[J].Dalton Transac-tions,2011,40( 19) : 5151-5158.
[2] Xiao X, Tu S, Lu M, et al. Discussion on the reaction mechanism of the photocatalytic degradation of organic contaminants from a viewpoint of semiconductor photo-induced electrocatalysis[J]. Applied Catalysis B Environmental, 2016, 198:124-132.
[3] Tu W, Zhou Y, Zou Z. Photocatalytic Conversion of CO2 into Renewable Hydrocarbon Fuels: State-of-the-Art Accomplishment, Challenges, and Prospects[J]. Cheminform, 2014, 26(27):4607-4626.