纯镍N4,N6无缝管毛细管
纯镍合金-上海叶钢金属集团有限公司-上海叶钢金属集团有限公司 点击了解更多

◆纯镍N4,N6无缝管 产品尺寸范围:
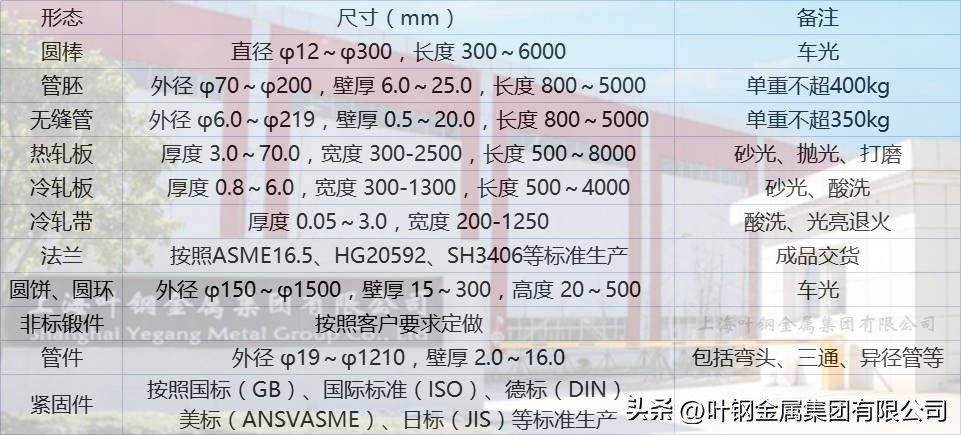
◆纯镍N4,N6无缝管 化学成分:
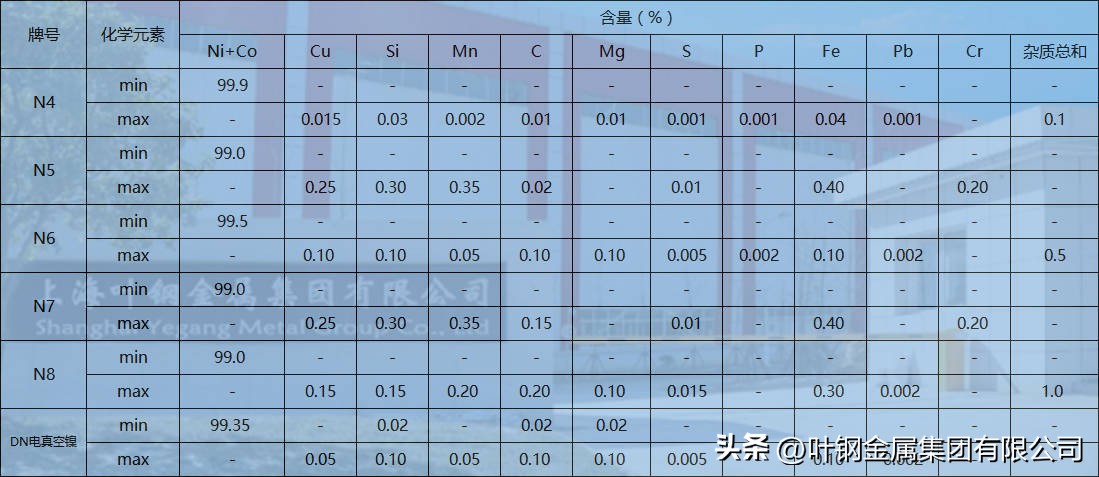
◆纯镍N4,N6无缝管 执行标准:
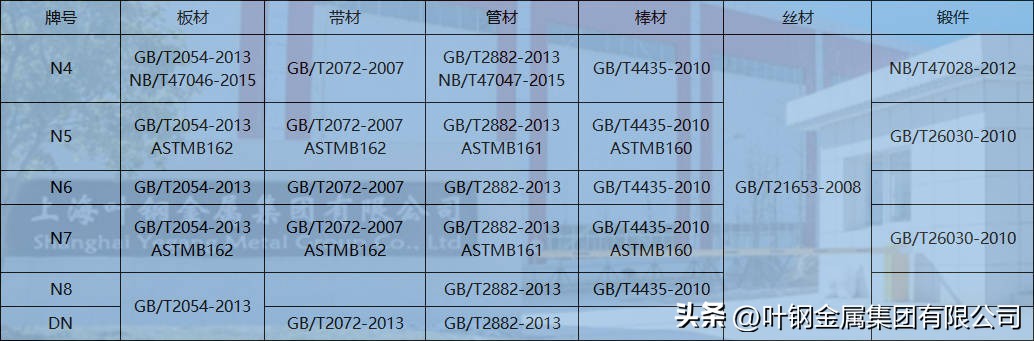
◆纯镍N4,N6无缝管 温室力学性能:
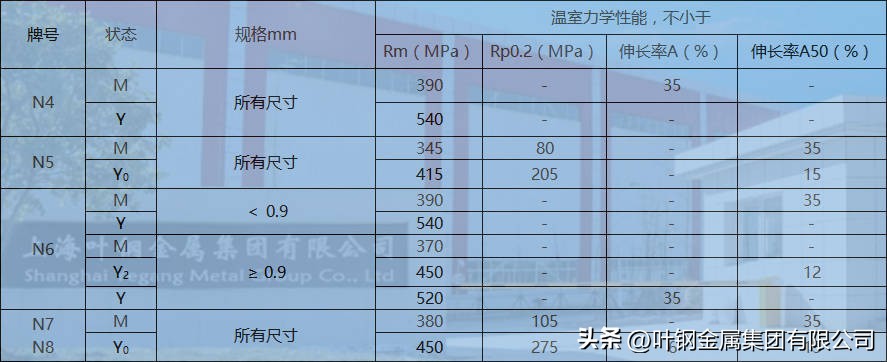
N6是镍质量分数在99。5%以上的纯镍材料。纯镍具有良好的力学性能和耐腐蚀性能,以及优良的塑性加工性能,与镍基合金相比纯镍具有更高的导电性、热导性和塑性。同时,它可被加工成各种不同形状的产品,被广泛应用于化工、电镀和电子领域。流变应力是影响金属塑性变形轧制压力变化的重要因素,而金属平面变形流变应力的测定能够正确揭示热轧塑性变形过程中材料组织和性能的变化及塑性变形规律。目前,有关纯镍的研究主要集中在镍基合金及纯镍冷变形行为的研究等方面,有关纯镍动态再结晶过程的模拟研究,有关纯镍冷变形行为的研究,有关工业纯镍的形变储能以及冷轧纯镍的显微硬度和微观组织结构的研究。但是,国内外有关纯镍热变形行为的研究很少。
纯镍N6热变形塑性加工图
加工图是由Parasad等基于动态材料模型开发的评价材料热加工性能的方法。该方法可以准确地描述金属高温塑性变形过程中。组织演变与变形参数之间的关系。同时,利用所建立的热变形塑性加工图,可以直观地展现出金属热变形过程中流变失稳区和合理加工区。从而为制定合理的金属热变形参数提供理论依据。
镍基合金是指以镍为基体,由铜、铬、钼等元素组成的合金,通常在 650~1000 ℃具有较高强度和抗氧化腐蚀能力。这种合金因优异的综合性能和耐各种酸腐蚀、应力腐蚀能力,在海洋、环保、能源、石油化工和食品等领域获得广泛应用。镍基合金之所以有优良的抗氧化性能,与基体 Ni 有密不可分的关系。纯镍具有良好的机械性能,易于冷加工,其加工性能与低碳钢相近,被广泛应用于板式换热器、制碱和化工装备等领域。N4 已在高达 1230 ℃的环境中使用,在酸性和碱性环境下,N4 均表现出了良好的耐蚀性。
纯镍分为加工纯镍和电镀镍两种。其中加工纯镍根据其镍含量分为二号镍、四号镍、六号镍、七号镍和八号镍。其供应的品种分别是二号镍、四号镍为板带材;六号镍和七号镍主要板带材、箔材、管材、棒材和线材为主;八号镍供应板材、棒材和线材。加工纯镍具有优良的性能,因此被广泛地应用于许多行业中,例如电子,机械设备制造,化学化工等行业中,还可以用于一些耐腐蚀的结构件等方面的制造,此外镍还是制造焊丝焊条时必须添加的金属原料。GB/T6516.1997标准是我国加工纯镍的国标。
N6是纯镍的一种又称六号镍,其中Ni和Co的含量大于99.5%,其他杂质含量不高于0.5%,N6具有耐酸碱的特性,在大气海洋中性能稳定,同时具有比较好的加工性能,较高的电真空性能,因此N6被广泛应用于化学化工、机械电子等行业,N6可以加工成板带材、线材、箔材等产品。
纯镍合金N4腐蚀性能
(1)热处理温度越高,N4 的耐蚀性越弱。N4 未经热处理的自腐蚀电位和点腐蚀电位分别为-0.55 V 和 0.254 V,均高于 N4 经不同温度热处理后的相关值。N4经 200℃热处理后,在 3.5%NaCl 溶液中腐蚀反应电阻和双电层电阻均最大,经300℃热处理后较小,经 400℃热处理后的最小。在 3.5%NaCl 溶液中浸泡 15 天后,未经热处理的 N4 主要以孔蚀为主。热处理温度越高,N4 表面生成的腐蚀产物越多,且腐蚀产物由枝晶状向絮状转变,腐蚀形式逐渐转为局部腐蚀。
(2)N4 在 5%NaCl 溶液中的腐蚀倾向最大,腐蚀速率最高,即 Cl-溶度越高,N4 耐蚀性越差。当 N4 浸泡在三种不同浓度的 NaCl 溶液中时,在 1%NaCl 溶液中的腐蚀速率较小,在 3.5%、5%NaCl 溶液中的腐蚀速率相对较大,其在 1%NaCl溶液中的自腐蚀电位最高,为-0.526 V;在 3.5%NaCl 溶液中的自腐蚀电位次之,为-0.640 V;在 5%NaCl 溶液中的自腐蚀电位最低,为-0.731 V。N4 在 5%NaCl 溶液中的腐蚀失重最多约 20 mg,在 1%NaCl 溶液中的腐蚀失重最少约 16 mg,腐蚀失重差值为 4 mg。且 Cl-浓度越高,N4 试样表面腐蚀孔数量越多,腐蚀孔径尺寸越大,在 5%NaCl 溶液中甚至出现了局部腐蚀现象。
(3)N4 在 15%NaOH 溶液中的腐蚀倾向最大,腐蚀速率最高,即 OH-浓度越高,N4 的腐蚀越严重。当 N4 浸泡在三种不同浓度的 NaOH 溶液中时,随着浸泡时间的延长,OH-在 N4 试样表面富集,导致腐蚀加快,腐蚀速率增大。N4 在15%NaOH 溶液中的容抗弧最小,在 10%NaOH 溶液中的次之,在 5%NaOH 溶液中的最大。在不同浓度 NaOH 溶液中浸泡 5 天后,N4 在 NaOH 溶液中均发生了腐蚀行为,OH-浓度越高,腐蚀失重越多,在 15%NaOH 溶液中腐蚀失重最多约 17 mg,在 5%NaOH 溶液中的腐蚀失重最少约 13 mg,腐蚀失重差值为 4 mg。且 OH-离子浓度越高,试样表面腐蚀坑和腐蚀产物越多。
(4)与OH-相比较,Cl-对 N4 的腐蚀行为影响更大。N4 在 5%NaCl和 5%NaOH溶液浸泡 5 天后,在 5%NaCl 溶液中的失重较多约 20.37 mg,在 5%NaOH 溶液中腐蚀失重较少约 15.17 mg,腐蚀失重差值为 5.2mg。在 5%NaCl 溶液中,N4 表面的腐蚀孔较多,且局部有深孔和裂痕,在 5%NaOH 溶液中,试样表面腐蚀并不明显,只在表面有少量杂质残留,且在 5%NaOH 溶液中,试样腐蚀情况相对较弱。
关于纯镍合金N6焊接工艺
(1) 采用填丝等离子焊接能实现N6纯镍的焊接,可以实现不开破口,单面焊双面成型,获得成型良好,外观饱满的焊缝。
(2) 填充ERNi-1焊丝的N6镍合金等离子焊接和不填丝等离子焊焊缝区与母材的相组成无本质区别,填充ERNi-1焊丝更利于消除镍合金焊接过程中的热裂纹和气孔倾向。
(3) N6填丝等离子焊焊接接头拉伸性能明显优于不填丝接头,填丝接头组织均匀、晶粒细小,抗拉强度为333Mpa达到母材的97.6%,延伸率为57%,断裂在热影响区;不填丝接头抗拉强度为240Mpa仅为母材的70.5%,延伸率为23%,断裂在焊缝中心。
(4) N6填丝接头焊缝区显微硬度明显高于不填丝接头焊缝,主要由于填丝接头焊缝区晶粒的细化,导致焊缝区显微硬度升高。
牌号有;N4 N6 N02201 N02200。
交货状态;M热加工状态。R冷加工状态。Y退火态超声波探伤。
公差;H7-H9 h7-h9
规格;镍板;厚度(0.5-20.0mm)宽度(200-1000mm)长度(500-2000mm)
镍棒;直径6-200mm*L
镍带/镍箔厚度(0.03-2mm)*宽度(1.5-300mm)*长度L
镍管;直径(3-110mm)*壁厚(0.8-8mm)*长度(200—8000mm)
镍丝:直径1.0/2.0/3.0/4.0mm*L
镍坩埚:容积10-300ml,整体,直筒或梯形,可以按照客户的要求定制加工。
执行标准;GB/T2072-93 GB2054-80 GB/2882-84 GB/8011-87 GB3120-82 GB4435-84.
广泛应用于;石油、化工、电子、机械设备、体育设备、科研领域。
拓展
镍(Nickel),是一种硬而有延展性并具有铁磁性的金属,它能够高度磨光和抗腐蚀。镍属于亲铁元素。地核主要由铁、镍元素组成。在地壳中铁镁质岩石含镍高于硅铝质岩石,例如橄榄岩含镍为花岗岩的1000倍,辉长岩含镍为花岗岩的80倍。
2017年10月27日,世界卫生组织国际癌症研究机构公布的致癌物清单初步整理参考,镍化合物在一类致癌物清单中,金属钴,金属镍和含有66-67%镍、13-16%铬和7%铁的合金粉末的体内植入异物、镍金属和镍合金在2B类致癌物清单中。
发现简史
陨石包含着铁和镍,早期它们被作为上好的铁使用。因为这种金属不生锈,它被秘鲁的土著看作是银。一种含有锌镍的合金被叫做白铜,在公元前200年的中国被使用。有些甚至延伸到了欧洲。
在1751年,工作于斯德哥尔摩(瑞典首都)的AlexFredrikCronstedt研究一种新的金属——叫做红砷镍矿(NiAs)——其来自瑞典的海尔辛兰的Los。他以为其包含铜,但他提取出的是一种新的金属,他宣布并命名为Nickel(镍)于1754年。许多化学家认为它是钴,砷,铁和铜的合金——这些元素以微量的污染物出现。直到1775年纯净的镍才被TorbernBergman制取,这才确认了它是一种元素。
矿产分布
世界上红土镍矿分布在赤道线南北30度以内的热带国家,集中分布在环太平洋的热带―亚热带地区,主要有:美洲的古巴、巴西;东南亚的印度尼西亚、菲律宾;大洋洲的澳大利亚、新喀里多尼亚、巴布亚新几内亚等。中国镍矿分布就大区来看,主要分布在西北、西南和东北,其保有储量占全国总储量的比例分别为76.8%、12.1%、4.9%。就各省(区)来看,甘肃储量最多,占全国镍矿总储量的62%,其次是*疆新**(11.6%)、云南(8.9%)、吉林(4.4%)、湖北(3.4%)和四川(3.3%)。其中甘肃金昌的铜镍共生矿床,镍资源储量巨大,仅次于加拿大萨德伯里镍矿,居世界第二,亚洲第一。
物理性质
有良好延展性,具有中等硬度。
镍是银白色金属,具有磁性和良好的可塑性。有好的耐腐蚀性,镍近似银白色、硬而有延展性并具有铁磁性的金属元素,它能够高度磨光和抗腐蚀。溶于硝酸后,呈绿色。主要用于合金(如镍钢和镍银)及用作催化剂(如兰尼镍,尤指用作氢化的催化剂) [3]
密度:8.902g/cm3 [2]
熔点:1453℃ [2]
沸点:2732℃ [2]
化学性质
外围电子排布3d84s2,位于第四周期第Ⅷ族。化学性质较活泼,但比铁稳定。室温时在空气中难氧化,不易与浓硝酸反应。细镍丝可燃,加热时与卤素反应,在稀酸中缓慢溶解。能吸收相当数量氢气。 [2]
镍不溶于水,常温下在潮湿空气中表面形成致密的氧化膜,能阻止本体金属继续氧化。在稀酸中可缓慢溶解,释放出氢气而产生绿色的正二价镍离子Ni2+;耐强碱。镍可以在纯氧中燃烧,发出耀眼的白光。同样的,镍也可以在氯气和氟气中燃烧。对氧化剂溶液包括硝酸在内,均不发生反应。镍是一个中等强度的还原剂。镍盐酸、硫酸、有机酸和碱性溶液对镍的浸蚀极慢。镍在稀硝酸缓慢溶解。发烟硝酸能使镍表面钝化而具有抗腐蚀性。镍同铂、钯一样,钝化时能吸收大量的氢,粒度越小,吸收量越大。
镍的重要盐类为硫酸镍和氯化镍。实验室中也常用到硝酸镍,带有结晶水,化学式为Ni(NO3)2·6H2O,绿色透明的颗粒,易吸收空气中的水蒸汽。与铁,钴相似,在常温下对水和空气都较稳定,能抗碱性腐蚀,故实验室中可以用镍煅钡熔融碱。硫酸镍(NiSO4)能与碱金属硫酸盐形成矾Ni(SO4)₂·6H2O(MI为碱金属离子)。+2价镍离子能形成配位化合物。常压下,镍即可与一氧化碳反应,形成剧毒的四羰基镍(Ni(CO)4),加热后它又会分解成金属镍和一氧化碳。 [4]
金属半径124.6皮米 [2]
第一电离能:741.1kJ/mol [2]
电负性:1.8 [2]
主要氧化数:+2、+3、+4 [2]
镍(Ⅱ)化合物
1.氧化镍:NiC2O4=NiO+CO+CO2
2.氢氧化镍:Ni2++2OH-=Ni(OH)2
3.硫酸镍:2Ni+2H2SO4+2HNO3=2NiSO4+NO2+NO+3H2O
NiO+H2SO4=NiSO4+H2O
NiCO3+H2SO4=NiSO4+CO2+H2O
4.卤化镍:NiF2、NiCl2、NiBr2、NiI2
镍(Ⅲ)化合物
1.氧化高镍
4NiO+O2=2Ni2O3
2Ni(OH)2+Br2+2OH-=Ni2O3+2Br-+3H2O
2Ni2O3+4H2SO4=4NiSO4+O2+4H2O
Ni2O3+6HCl=2NiCl2+Cl2+3H2O
2.氢氧化高镍
4NiCO3+O2=2Ni2O3+4CO2
2Ni(OH)2+NaClO+H2O=2Ni(OH)3+NaCl
2Ni(OH)3+6HCl=2NiCl2+Cl2+6H2O
配合物
1.氨配位化合物:[Ni(NH3)6]2+
2.氰配位化合物:[Ni(CN)4]2-
3.螯合物:[Ni(en)3]2+
4.羰基配位化合物
(a)Ni(CO)4;
(b)(C2H5)2N