编者按:原发性先天性青光眼是一种严重的渐进性神经退行性致盲性疾病,也是60岁以上人群失明的最常见原因之一,其特征表现为TM和Schlemm's管(SC)的发育缺陷以及房水流出通道受阻。有研究证实ANGPT1和SVEP1基因变异可被确定为原发性开角型角青光眼(POAG)的等位风险基因。ANGPT1-TEK信号通路在小鼠SC发育中发挥着重要作用,也是维持成年小鼠和非人类灵长类动物IOP平衡的重要调节剂,因此,抑制ANGPT-TEK信号可导致IOP迅速升高并诱发青光眼。此外,SC和TM的调节通路或许可作为调节房水流出并降低IOP的治疗目标,TM中表达的SVEP1基因对淋巴的发育至关重要,也与PCG以及TEK功能变异的异质性缺失具有相关性。近期发表于Nature Communications杂志上的一项研究带来了一个好消息,该研究在小鼠模型中发现了一种可有效促进房水流出的有效靶向疗法,这种新方法有望扭转青光眼患者潜在的解剖学缺陷。
循循渐进:青光眼的探索性研究
高眼压是导致青光眼疾病进展的一项主要危险因素,目前青光眼治疗的主要手段是降眼压治疗。降眼压眼药水和激光治疗均可有效降低IOP并延缓疾病进展,但并不能完全治愈青光眼,原发性先天性青光眼则只能选择手术治疗。多数患者常需要两种或两种以上药物联合治疗,且药物治疗也有个体差异性。因此,探索青光眼的有效治疗方案迫在眉睫。
研究一:Angpt1的表达
对实验小鼠进行ANGPT1注射治疗后收集研究数据并进行分析。研究发现,Angpt1+NC模型中虹膜Angpt1表达几乎为零,视网膜中Angpt1表达轻度减少;除视网膜内界膜外,Angpt1可在神经上皮无长突细胞中表达。尽管对TEEK和ANGPT2信号的依赖性很强,野生型小鼠视网膜中Angpt1表达极低,但1型视网膜血管生成并不需要Angpt1。
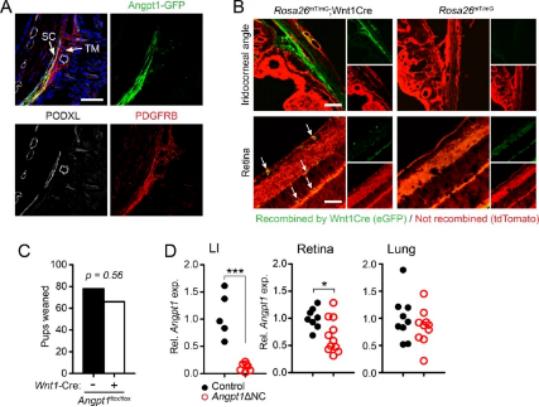
图1. A未检测到Angpt1表达;B重组仅限于视网膜内膜;C特定敲除(Angpt1+NC)小鼠;D 12 周Angpt1 +NC小鼠Angpt1mRNA表达显著减少。视网膜中观察到Angpt1mRNA表达有所减少,而肺等实体器官Angpt1表达方式无改变。
研究二:验证Angpt1+NC小鼠是否存在青光眼迹象
研究结果显示,7 周大Angpt1+NC小鼠模型中IOP升高且眼轴变长,15周大时SC区域大幅减少。因此,TM 细胞ANGPT1的分泌对SC形成和维持IOP 平衡至关重要。
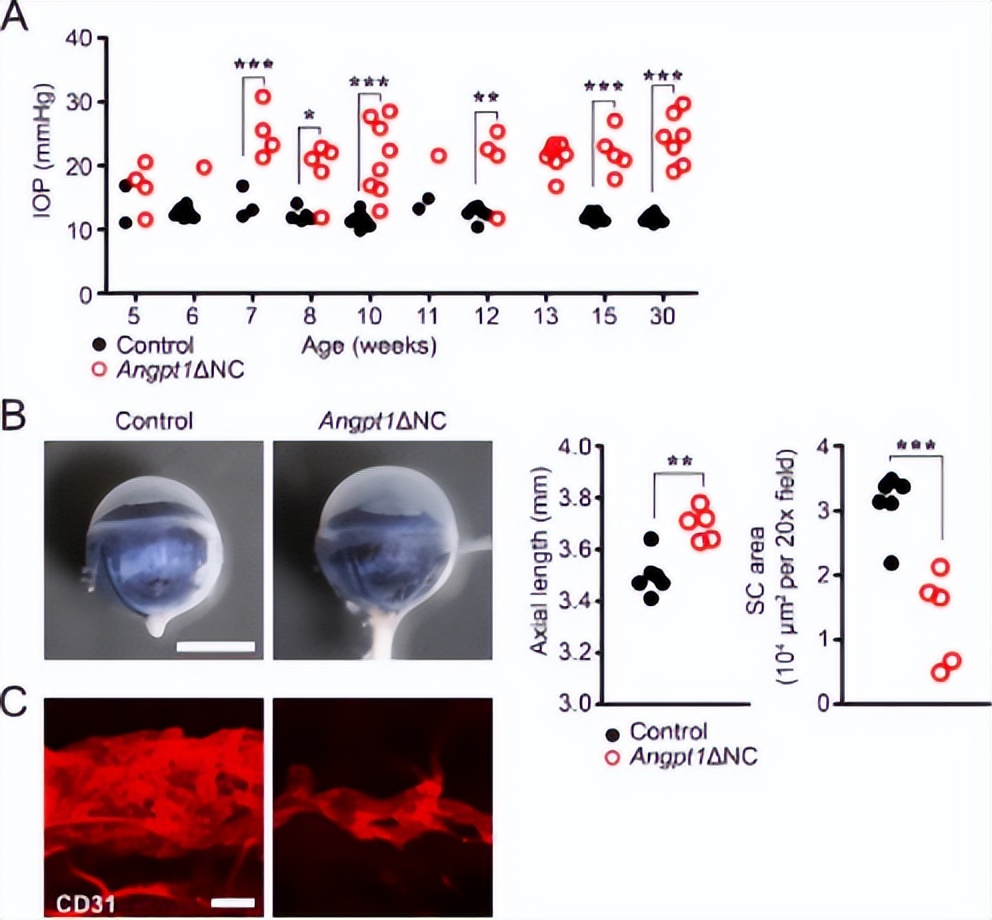
图3. 15周大Angpt1+NC小鼠视网膜(A)BRN3A和(B)BRN3B阳性RGCs细胞核的数量减少。这种减少在外周视网膜中尤为明显。C Angpt1+NC小鼠中观察到RGCs减少。D 15周内Angpt1+NC小鼠视网膜直径基本保持不变。
研究三:Angpt1+NC小鼠的青光眼表型
研究证实,高眼压型青光眼的视力丧失与视网膜神经节细胞(RGCs)凋亡有关。该研究对RGC进行了计数统计后发现,5天时RGC数量无明显变化,15周时Angpt1+NC小鼠RGC显著减少,且在外周视网膜中表现尤为明显。研究中还对视网膜血管进行了检测以确认Angpt1+NC小鼠RGC的减少是否由IOP升高所致而与视网膜缺血无关。
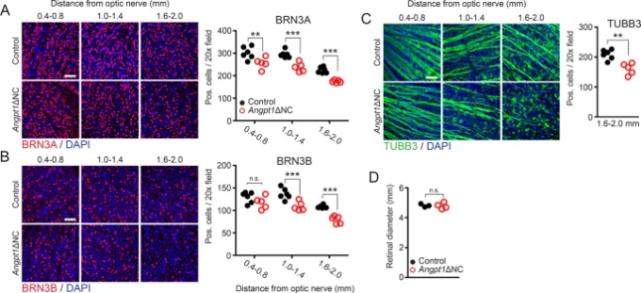
图3. 15周大Angpt1+NC小鼠视网膜(A)BRN3A和(B)BRN3B阳性RGCs细胞核的数量减少。这种减少在外周视网膜中尤为明显。C Angpt1+NC小鼠中观察到RGCs减少。D 15周内Angpt1+NC小鼠视网膜直径基本保持不变。
研究四:一种与PCG相关的新基因-Svep1
最新观点称SC可被认为是一种独特的"混合"内皮。SC同时具有血管和淋巴管特性,且淋巴信号分子(如PROX1和FLT4)在SC调节中具有重要作用。SVEP1或可出现导致编码淋巴管发育和瓣膜形成所需的细胞外基质蛋白相关的功能缺失的基因变异,并推测该突变可作为改善PCG的“修饰剂”。GWAS已确定SVEP1变异是POAG 的等位风险基因,进一步支持了SVEP1在平衡IOP中的调节作用。假设SVEP1信号通路是TM-SC的一种联系通路,且在TM和SC内皮中SVEP1表达丰富(图4A)。成功建立小鼠模型后发现,随着生长可表现出严重低形态SC缺乏PROX1表达(图4B、4C)以及四肢血管杂乱无章(图4D),在眼淋巴血管中仅观察到部分保留的区域。4周开始,实验小鼠出现IOP升高趋势,因此研究确定了SVEP1对IOP平衡的重要性。
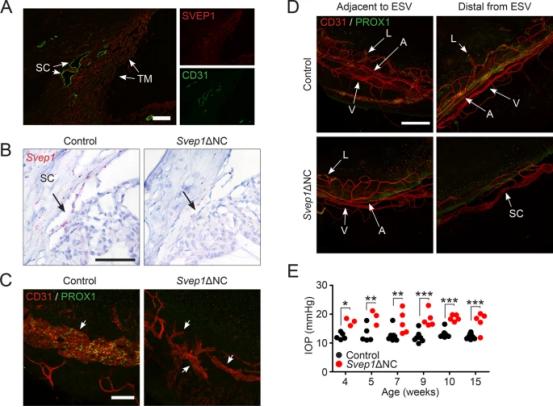
图4. A人角膜免疫染色,在TM和SC内皮中观察到SVEP1表达。B Svep1+NC小鼠Svep1表达损失通过原位杂交得到确认。产后第10天Svep1+NC模型,一个畸形的SC的形成没有明显的PROX1。D除SC形成缺陷外,Svep1+NC小鼠中还发现了四肢血管和淋巴网缺陷,其在Svep1突变体中杂乱无章。确认这种畸形SC和杂乱的畸形外流通路提供了不足的排水功能, 4周大开始,眼压升高。
研究五:神经峰-SC的细胞基础
该研究对所建立的小鼠模型,进行分析细胞学分析后发现,在Angpt1+NC模型中检测到的Angpt1表达细胞很少,且在虹膜角/边缘区域的Angpt1表达细胞来自神经波峰。此外,该研究还进行了SC内皮细胞的识别、集群分类、TM细胞群的识别等。
研究六:相关基因和通路的表达
该研究在SC内皮细胞中发现了21个基因,在假定TM细胞群中发现了30个基因。在SC或TM中检测到的一些具有已知表达的基因在两个细胞群中都超过了阈值,且它们的表达出现严重偏斜。
新观点:Hepta-ANGPT1或可作为青光眼治疗的潜在有效目标
ANGPT-TEK信号通路可增强SC功能并促进房水流出。最近研发的一种高效ANGPT1-mimetic融合蛋白,可在体内和体外有力地激活TEEK。对小鼠模型研究发现,注射融合蛋白后SC区域急剧增加,PROX1表达水平升高,血管形态依然正常,这表明其作用特定局限于SC。重复Angpt1+NC小鼠实验后发现,模型中出现低形态SC,其PROX1染色减少或缺失,因此判断Angpt1-mimetic在Angpt1+NC小鼠中诱导的内皮结构并非完全成熟的SC。为了确定在停止Hepta-ANGPT1 治疗后是否对成年小鼠的房水流出通路具有持久影响,该研究建立相关动物模型并分析数据后发现,停止治疗后实验小鼠IOP降低。因此,研究推测Hepta-ANGPT1 治疗具有持久效果。
虽然之前有研究描述过TM和SC中ANGPT1的表达,但均依赖于全身删除或阻断抗体,而不是组织特定性删除,因此ANGPT1的细胞起源未经验证。该研究中利用经神经波峰特异性删除Angpt1,以确认SC调节ANGPT1的TM起源。该研究提出可将TEK 激活作为治疗策略。对SC分子特性、发育和功能的更深入了解,有利于为研究人员针对SC和常规房水流出通路或内皮特定信号通路研发提供新思路,这些药物将直接通过广泛活性化合物(如Rho激酶*制剂抑**、作用素去聚合剂等药物)发挥作用。现阶段,通过 ANGPT-TEK 通路达到治疗效果是较为先进的一项研究。
最近的一项药理动力学研究表明,在静脉注射Hepta-ANGPT1 3天后,兔房水中Hepta-ANGPT1水平很高,该研究数据与之前的研究数据具有一致性。Hepta-ANGPT1治疗期间或注射后,不会诱发SC或其他部位病理性血管的生成。此外,该研究种结果还表明,ANGPT1和SVEP1是TM 的衍生分子,也是SC的基本调节器,其中ANGPT1可诱导SC发育和生长。这些信号分子或可成为青光眼的新型疗法。数据还显示其他几个信号分子也与青光眼有关,不久的未来也可为针对房水流出途径的研究和药物开发提供极大的可能性。
小结
有小鼠模型显示敲除Angpt1或Svep1可出现类青光眼表现。大量研究已证实TM的表达是SC的基本驱动力。现已成功利用基因编辑建立类原发性先天性青光眼的小鼠模型,并探索出通过一种新型、持久、无毒的蛋白质治疗(Hepta-ANGPT1),或可作为预防青光眼的形成并降低IOP的有效手段。Susan Quaggin教授指出,未来可进一步研发适宜的蛋白质输送系统并将其投产。此外,科学家还利用生物信息学和单细胞RNA序列数据来理解和识别青光眼途径,这些途径可在未来进一步探索以达到实现疾病治疗的目标。促进改善存在SC生长缺陷的治疗是实现青光眼治愈的第一步,该研究探索性识别出不同TM和SC细胞群,确定了TM-SC信号通路,证实了血管生成素信号对SC的重要性。此外,该研究突出了 ANGPT1-TEK信号和 TM-SC 信号在平衡IOP中的核心作用,并为青光眼治疗提供了新的靶向候选目标。
(来源:《国际眼科时讯》编辑部)
SC 信号在平衡IOP中的核心作用,并为青光眼治疗提供了新的靶向候选目标。
(来源:《国际眼科时讯》编辑部)